Недавно исследовательская группа Чэнь Чжэна из Центра наук о жизнедеятельности ХПУ выявила важный функциональный механизм РНК-метилтрансферазы METL3 в возникновении и развитии неалкогольного стеатогепатита (NASH). Научная статья «Метилтрансфераза METTL3 отрицательно регулирует прогрессирование неалкогольного стеатогепатита (NASH)», опубликована в престижном журнале «Nature Communications».
Около 25% нормальной неалкогольной жировой печени (NAFL) разовьется в неалкогольный стеатогепатит (NASH), а NASH в дальнейшем перерастет в цирроз и рак печени. Какие гены регулируют переход от NAFL к NASH, неясно. Группа Чэнь Чжэна обнаружила, что РНК-метилтрансфераза METTL3 играет важную роль в этом процессе. У мышей с нокаутом специфичного для печени гена Mettl3 развился фенотип NASH при кормлении с высоким содержанием жиров, что проявлялось в повышении АЛТ, более выраженном ожирении печени, повреждении печени, гепатите и фиброзе печени, но у контрольных мышей Mettl3flox/flox не проявлялся фенотип NASH. Мыши Mettl3-HKO более чувствительны к NASH, индуцированному MCD, и имеют более тяжелый NASH.
Нокаут специфичного для печени гена Mettl3 способствует экспрессии CD36, увеличивает поглощение свободных жирных кислот и приводит к накоплению липидов в печени. Такой нокаут также способствует экспрессии CCl2, что приводит к гепатиту и повреждению печени. Опосредованное CD36 увеличение поглощения свободных жирных кислот и вызванное CCL2 воспаление способствовали прогрессированию NASH у мышей Mettl3-HKO. Антитела, нейтрализующие CD36 и CCL2, могут облегчить MCD-индуцированный мышами Mettl3-HKO NASH. Специфическая для печени сверхэкспрессия METL3 может подавлять экспрессию CD36 и CCL2 и облегчать MCD-индуцированный NASH.
Результаты RNA-seq, ATAC-seq и m6ARIP-seq показывают, что METL3 регулирует доступное состояние хромосомы и транскрипцию промоторных областей Cd36 и Ccl2 и не зависит от активности метилтрансферазы METL3. METTL3 может регулировать ацетилирование H3K9 и H3K27 в промоторных областях Cd36 и Ccl2 путем связывания с HDAC1/2 (гистондеацетилаза). Ингибиторы HDAC1/2 (TSA или ромидепсин) могут частично обратить вспять ингибирующее действие METL3 на экспрессию Cd36 и Ccl2.
Кроме того, в случае NASH, METL3 в клеточном ядре снижается, а METTL3 в цитоплазме увеличивается, а взаимодействие между METTL3 и HDAC1/2 ослабляется. Клеточное ядро/плазменный челнок METTL3 связан с TNFα/CDK9- опосредованным фосфорилированием.
Эти результаты раскрывают важный механизм METL3 в патогенезе NASH и обеспечивают потенциальную лекарственную мишень для лечения NASH.
Ли Синьчжи, постдокторат Центра наук о жизнедеятельности ХПУ, и докторант Юань Бинюань являются первыми соавторами статьи, а профессор-исследователь Чэн Чжэн – автором-корреспондентом статьи. Лу Минь, старший инженер Центра экспериментального обучения Института наук о жизнедеятельности, и аспиранты исследовательской группы Ван Юйцинь, Дин На, Лю Чуньхун и Гао Мин приняли участие в исследовании этого проекта. Этот проект также активно поддержали доктор Яо Чжичэн из Третьей больницы Университета Сунь Ятсена, аспирант Чжан Шиянь и профессор-исследователь Чжао Юйцзюнь из Шанхайского института медицинской материи Китайской академии наук и профессор-исследователь Се Ливэй из Гуандунского института микробиологии. Этот проект финансировался Государственным фондом естественных наук Китая и средствами «двойного первого класса» ХПУ.
ССЫЛКА НА ОРИГИНАЛ СТАТЬИ:https://www.nature.com/articles/s41467-021-27539-3
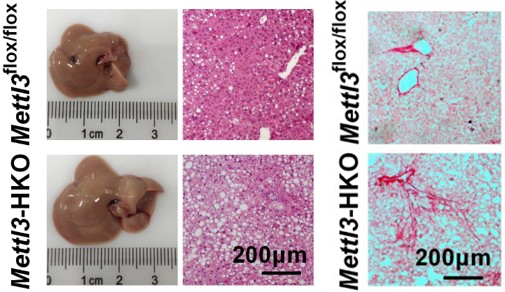
Мыши Mettl3-HKO имеют более тяжелую жировую дистрофию печени и фиброз печени при кормлении с высоким содержанием жиров.
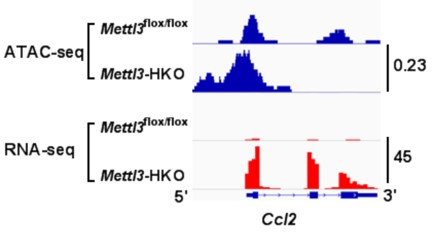
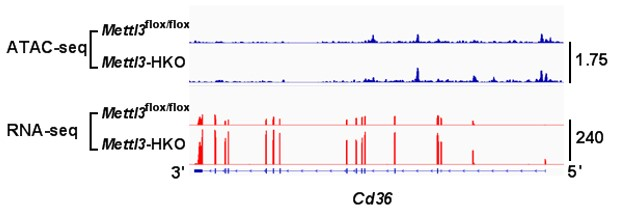
ATAC-seq и RNA-seq показывают, что нокаут специфичного для печени гена Mettl3 способствует доступности хромосомы и транскрипции в промоторных областях Cd36 и Ccl2.

